气体制备、净化与收集 实验室操作全解析
在化学实验室中,气体的制备、净化和收集是基础且关键的实验操作。掌握这一系列流程的原理与方法,是进行后续性质研究或实际应用的前提。本文将系统性地阐述这三个环节的核心要点。
一、气体制备:方法与选择
气体制备的核心是根据所需气体的化学性质,选择合适的反应原理和发生装置。主要方法包括:
- 固体加热法:适用于热稳定性较差、受热易分解的固体反应物,如加热高锰酸钾制取氧气(2KMnO₄ → K₂MnO₄ + MnO₂ + O₂↑)。常用装置为带有酒精灯和导管的硬质玻璃管。
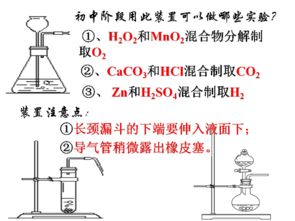
- 固液常温法:这是最常用的方法,适用于块状或颗粒状固体与液体在不加热条件下反应,如锌粒与稀硫酸反应制取氢气(Zn + H₂SO₄ → ZnSO₄ + H₂↑)。常用装置为简易启普发生器或其变体。
- 液液加热法:适用于两种或多种液体需要加热才能顺利反应的体系,如乙醇与浓硫酸在170℃下反应制备乙烯。此时需使用带有温度计和分液漏斗的圆底烧瓶装置。
选择依据:首要考虑反应物的状态和反应条件(是否需要加热),其次是反应速率可控性、安全性以及装置简易程度。
二、气体净化:除去杂质
由于反应物不纯、副反应或装置带入水汽等原因,生成的气体常含有杂质。净化目的就是获得纯净的目标气体。净化操作通常在制备之后、收集之前进行,通过洗气瓶或干燥管实现。
- 除杂原则:
- 不减少:净化试剂不能与目标气体发生反应。
- 不引入:不能引入新的杂质气体。
- 易分离:最好通过一次洗气或干燥即可完成。
- 常见净化试剂与方法:
- 除酸性杂质(如HCl、CO₂、SO₂):可用碱性溶液(如NaOH溶液)或固体碱石灰。
- 除碱性杂质(如NH₃):可用酸性溶液(如稀硫酸)。
- 除还原性杂质(如H₂S):可用硫酸铜溶液或高锰酸钾溶液。
- 除水蒸气(干燥):根据气体性质选择干燥剂。酸性干燥剂(如浓硫酸、五氧化二磷)不能干燥碱性气体(如NH₃);碱性干燥剂(如碱石灰、固体NaOH)不能干燥酸性气体(如CO₂、SO₂、HCl);中性干燥剂(如无水氯化钙)应用较广,但不能干燥NH₃。
操作顺序:一般先除杂后干燥。若用水溶液除杂,气体出来时会带出水蒸气,因此干燥必须放在最后一步。
三、气体收集:依据性质定方法
收集方法的选择完全取决于气体本身的物理和化学性质。
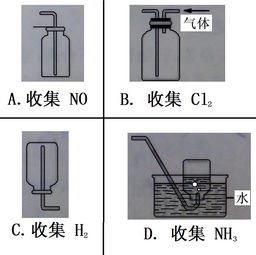
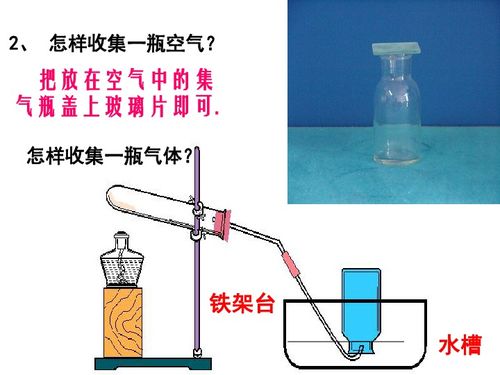
- 排水集气法:
- 适用气体:不易溶于水且不与水反应的气体,如O₂、H₂、N₂、CO、CH₄等。
- 优点:收集到的气体纯度高、浓度大。
- 操作:集气瓶装满水倒扣在水槽中,导管伸入瓶口。
- 向上排空气法:
- 适用气体:密度大于空气(平均分子量 > 29)且不与空气中成分反应的气体,如CO₂、SO₂、HCl、Cl₂(通常用排饱和食盐水法更好)等。
- 操作:导管伸入集气瓶底部,利用气体密度大而下沉,将空气从瓶口向上排出。
- 向下排空气法:
- 适用气体:密度小于空气(平均分子量 < 29)且不与空气中成分反应的气体,如H₂、NH₃、CH₄等。
- 操作:导管伸入集气瓶底部,利用气体密度小而上升,将空气从瓶口向下排出。
注意事项:排空气法收集气体时,导管应尽可能伸到集气瓶底部,以利于排尽空气;同时可在瓶口进行验满操作。
四、实验流程整合与安全
一个完整的气体制备实验,需将上述三个环节有序串联:发生装置 → 净化装置 → 干燥装置 → 收集装置。若气体有毒或有害(如Cl₂、SO₂),必须在最后连接尾气处理装置(如用NaOH溶液吸收)。
安全始终是第一要务。实验前必须明确气体的毒性、可燃性、爆炸极限等;检查装置气密性;加热反应时防止液体倒吸;易燃易爆气体(如H₂)收集或实验时需远离明火。
气体制备、净化与收集是一个环环相扣的系统工程。深入理解每一步的原理,并严格遵循操作规范,是实验成功与人员安全的根本保障。
如若转载,请注明出处:http://www.tangkeqx.com/product/70.html
更新时间:2026-05-22 12:05:36