化学实验设计专题 常见气体的制取、净化、收集与验证

化学实验是探索物质世界的重要手段,其中气体的制取、净化、收集与验证是核心实验技能。掌握这些知识,不仅有助于理解化学反应原理,更能提升实验设计与分析能力。本文将对氧气(O₂)、氢气(H₂)、二氧化碳(CO₂)、氨气(NH₃)、氯气(Cl₂)等常见气体的相关实验进行系统复习。
一、 气体的制取
制取气体需根据反应原理、药品状态及反应条件选择合适装置。
- 固体加热型:适用于反应物为固体、需加热的反应,如用高锰酸钾或氯酸钾与二氧化锰制氧气。装置特点:试管口略向下倾斜,防止冷凝水倒流。
- 固液不加热型:适用于块状固体与液体在不加热条件下反应,如用锌粒与稀硫酸制氢气、用大理石(或石灰石)与稀盐酸制二氧化碳。常用装置为简易发生器或启普发生器,能随时控制反应进行。
- 固液或液液加热型:适用于反应物需在加热条件下反应,如用氯化铵与氢氧化钙固体加热制氨气、用二氧化锰与浓盐酸加热制氯气。装置中需包含酒精灯,且常需分液漏斗控制液体加入。
二、 气体的净化(除杂与干燥)
制得的气体常含杂质(如水蒸气、酸雾或其他气体),需根据杂质性质选择净化试剂与装置。基本原则是:先除杂,后干燥;除杂试剂不与目标气体反应。
- 除杂:选择能与杂质反应而不与目标气体反应的试剂。如用饱和碳酸氢钠溶液除去CO₂中混有的HCl气体(HCl与NaHCO₃反应生成CO₂),用灼热的铜网除去O₂中混有的H₂。
- 干燥:选用合适的干燥剂吸收水蒸气。常见干燥剂有:浓硫酸(酸性,可干燥O₂、H₂、CO₂、Cl₂等,不能干燥碱性气体如NH₃)、碱石灰(碱性,可干燥NH₃,不能干燥酸性气体如CO₂、Cl₂)、无水氯化钙(中性,可干燥多数气体,但不能干燥NH₃)。装置通常为洗气瓶(液体干燥剂)或干燥管/U形管(固体干燥剂)。
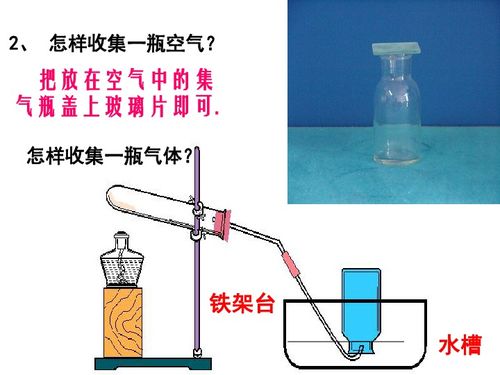
三、 气体的收集
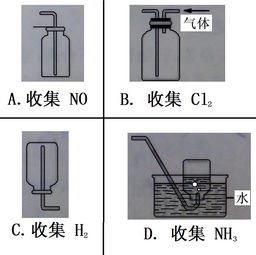
收集方法取决于气体的密度(与空气比较)和溶解性。
- 排水法:适用于不易溶于水且不与水反应的气体,如O₂、H₂。此法收集的气体纯度较高。
- 向上排空气法:适用于密度比空气大(相对分子质量 > 29)的气体,如CO₂、Cl₂。集气瓶口向上。
- 向下排空气法:适用于密度比空气小(相对分子质量 < 29)且不与空气反应的气体,如H₂、NH₃。集气瓶口向下。
四、 气体的验证(检验与验满)
验证包括对气体身份的检验(是什么气体)和收集满的确认(验满)。
- 氧气(O₂):检验——将带火星的木条伸入集气瓶,木条复燃。验满(排空气法)——将带火星的木条置于瓶口,木条复燃。
- 氢气(H₂):检验——点燃,产生淡蓝色火焰,干冷烧杯罩在火焰上方有水滴生成(点燃前务必验纯)。
- 二氧化碳(CO₂):检验——通入澄清石灰水,石灰水变浑浊。验满——将燃着的木条置于瓶口,木条熄灭。
- 氨气(NH₃):检验——用湿润的红色石蕊试纸靠近,试纸变蓝;或蘸有浓盐酸的玻璃棒靠近,产生大量白烟(NH₄Cl)。
- 氯气(Cl₂):检验——用湿润的淀粉碘化钾试纸靠近,试纸变蓝。
五、 综合设计与注意事项
设计完整的气体制备实验时,需将上述环节有序组合:制取装置 → 净化装置 → 收集装置 → 尾气处理装置(有毒气体如Cl₂需用NaOH溶液吸收)。务必注意操作安全,如点燃H₂前必须验纯,加热制气时防止倒吸,处理有毒气体时注意通风与吸收。
通过系统梳理常见气体的制取、净化、收集与验证,我们能够构建清晰的实验知识网络,提升解决综合性实验问题的能力。在实践中,需灵活运用原理,严谨设计步骤,方能确保实验的成功与安全。
如若转载,请注明出处:http://www.tangkeqx.com/product/69.html
更新时间:2026-05-22 19:23:57